_______________________________________________________________
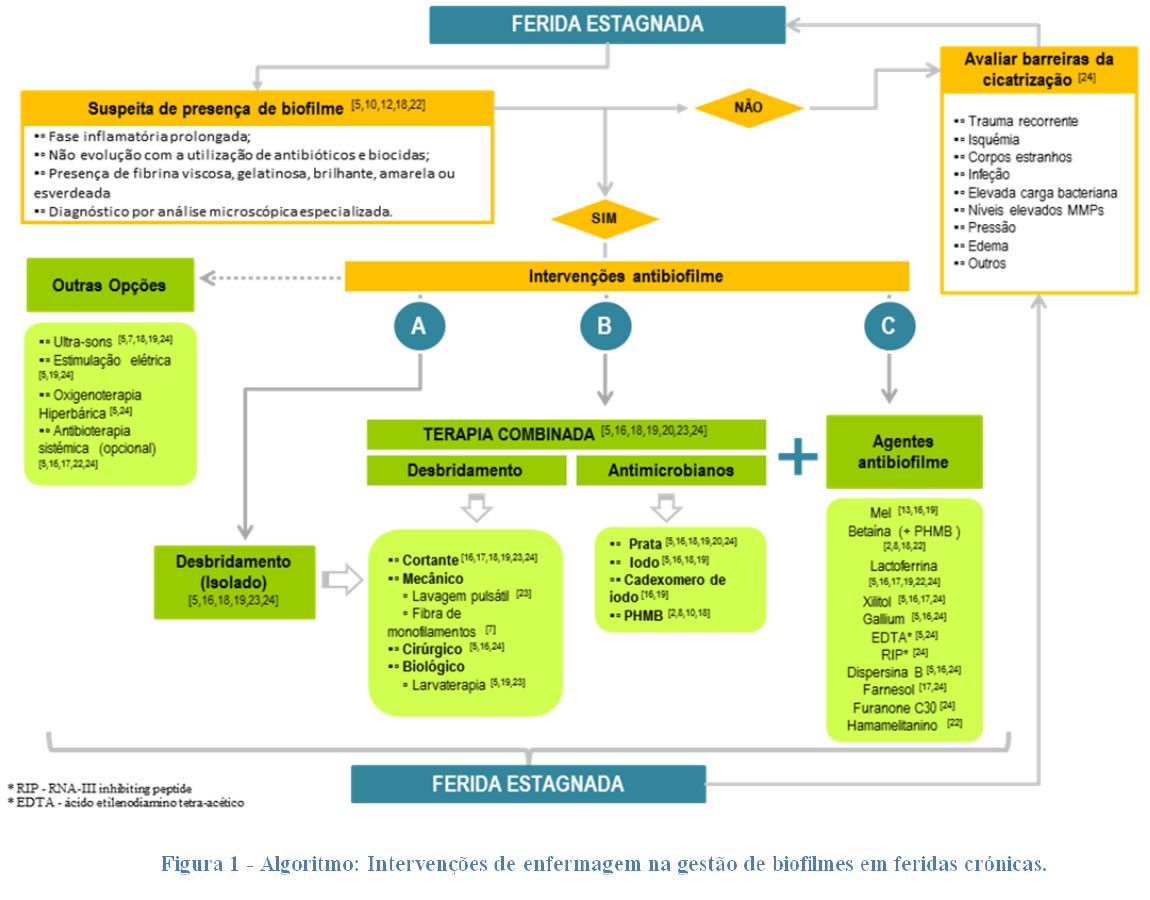
SILVER CALCIUM-ALGINATE MATRIX IN INFECTED WOUNDS: CASE STUDIES
MATRIZ DE ALGINATO DE CÁLCIO CON PLATA EN HERIDAS INFECTADAS: ESTUDIOS DE CASO
_______________________________________________________________
AUTORES: Vítor Santos, Ana Sofia Santos, Elsa Menoita
Resumo
A identificação e tratamento da infecção nas feridas varia e nem sempre é um processo fácil, no entanto, a base do diagnóstico deve assentar na clinica, na identificação dos sinais e sintomas, embora possa em alguns casos ser necessário recorrer a exames microbiológicos. Para o tratamento da infecção são várias as opções disponíveis, sendo todas elas válidas e eficazes. No entanto na última década, o dominio em termos de tratamento local da infecção em feridas, pertence aos apósitos com prata. Esta hegemonia tem vindo a ser desafiada nos últimos tempos, por apósitos alternativos e principios activos alternativos. Assim o sendo os pensos com prata, atravessaram um processo evolutivo, que os coloca em condições de continuar como uma opção extremamente válida e eficaz no tratamento da infecção em feridas. Um exemplo deste processo é o apósito que consiste numa matriz de alginato com prata iónica, que para além da apresentação associada a espuma de poliuretano, passa a ter um pelicula de matriz de alginato com prata iónica e uma versão em pasta. Com este artigo pretendo dar a conhecer os primeiros estudos de caso efectuados em Portugal, onde se evidencia a eficácia destes apósitos no tratamento da infecção de feridas crónicas.
Palavras Chave: Infecção, feridas crónicas, estudo de caso
_______________________________________________________________
Abstract
The identification and treatment of infection in wounds varies and is not always an easy process, however, it must be based on clinical diagnosis, identification of signs and symptoms, but may in some cases be necessary to run microbiological tests. For treatment of infection are several options available, all of which are valid and effective. However in the last decade, silver dressings dominated, the field in terms of local treatment of infection in wounds. This hegemony has been challenged in recent times by alternative dressings with new alternative substances. As so, the silver dressings crossed an evolutionary process, which puts them in a position to continue as an extremely valuable and effective option to treat wound infection. An example of this process is the dressing consisting of an alginate matrix with silver ion, which in addition to the presentation associated with polyurethane foam, is now accompanied by a film of alginate matrix with silver ion and a paste version. With this article I intend to make known the first case studies carried out in Portugal, where it shows the efficacy of these dressings in the treatment of chronic wound infection.
Keywords: Infection, chronic wounds, case study
_______________________________________________________________
Enquadramento da Problemática
A prata é um elemento que tem sido utilizado com intenções curativas há mais de 2000 anos. De acordo com Grahan, citado por Ousey (2009), a prata é uma terapia antiga tendo sido já utilizada pelos romanos para a purificação da água e, no século XVIII, como agente antibacteriano. Os navegadores portugueses na altura dos descobrimentos foram mesmo “pioneiros” ao utilizarem peças de prata nos barris de água, de modo a que se mantivesse potável ao longo dos vários meses de viagem no mar. Já no século XIX, descobriu-se que os iões de prata têm propriedades antimicrobianas e que uma solução altamente diluida de nitrato de prata inibe fortemente o crescimento de Staphylococcus aureus (Klasen citado por Ousey, 2009). A sua utilização desde o século XIX, prende-se com o facto de possuir fortes propriedades antimicrobianas, o que potenciou a sua importação para a vertente medicinal. No século XX, segundo White citado por Ousey (2009), a prata e os seus compostos, foram então utilizados por profissionais de saúde para combater infeções bacterianas em feridas agudas e crónicas. Ao longo dos últimos 40 anos, aumentou ainda mais o interesse da utilização da prata em produtos de cuidados a feridas, devido ao aumento da resistência bacteriana aos antibióticos (Ousey, 2009). Desde a década de 60 do século XX, com o uso tópico da prata com a intenção de tratar feridas, nomeadamente queimaduras infectadas, através de um creme de nitrato de prata a 0,5%, de forma eficaz, a popularidade da prata tem vindo a aumentar, e muito se deve à sua eficácia no tratamento de feridas infectadas. A prata actua no metabolismo bacteriano, inibindo assim a sua replicação e a possibilidade de desenvolver resistência, actuando em vários microrganismos, nomeadamente, bactérias aeróbias, anaeróbias, gram-positivas (Staphylococcus aureus, Streptococcus hemolyticus), gram-negativas (Pseudomonas aeruginosas), fungos e vírus. A prata apresenta-se sobre a forma de apósitos e cremes, pelo que a sua concentração varia. É, então, fundamental compreender a importância das concentrações de prata aplicadas na ferida, pois uma quantidade excessiva pode levar a atrasos na cicatrização. Sabemos hoje em dia que a prata mantém a sua capacidade antibacteriana, com baixas concentrações (0,001-0,06 partes por milhão), diminuindo assim o risco de toxidade (Shu-Fen, 2008).
A prata é encontrada como uma série de compostos, mas são os iões Ag+, o agente antimicrobiano ativo. Na forma metálica (elementar), para se tornar bactericida, a prata (átomo Ag) tem que se ionizar, ou seja, perder um eletrão e tornar-se um ião de prata (Ag+). Isto acontece em contacto com o ar, mas ainda mais facilmente em exposição aquosa. Já os compostos que contêm iões de prata, têm a vantagem de a mesma se destacar do composto que a transporta com maior facilidade quando exposta a ambientes húmidos (Leaper, et al; 2012). Assim, quando o apósito entra em contacto com o exsudado da ferida ocorre troca de iões Ag+, com os de sódio Na +, presentes no exsudado.
Os iões Ag+ ligam-se à membrana das células bacterianas causando rutura da parede das mesmas. Perante isto, os iões de prata são transportados para o interior da célula e perturbam as funções da mesma ligando-se às proteínas de ADN e ARN e, interferem na produção de energia, função da enzima e replicação celular. (Leaper, et al,2012 e Hampton, 2010). Apesar de ainda não existirem Estudos controlados randomizados que o comprovem, vários estudos experimentais em animais revelaram que, ao reduzir a carga bacteriana, a prata reduz a ação anti-inflamatória, através da redução da atividade das metaloproteinases (interfere com a actividade do ião de Zinco), citoquinas pró-inflamatória e apoptose celular (Leaper, et al,2012)
A prata pode ser incorporada em pensos através de várias formas diferentes, principalmente sob a forma de prata elementar ou no estado iónico. Ag+ é a forma iónica, a qual tem demonstrado possuir um amplo efeito antimicrobiano. Existem poucos pensos com prata no estado iónico, sendo que nesta categoria se pode incluir a matriz de alginato de cálcio com prata iónica que pode ter 3 formas de apresentação: Pelicula simples, película associada a espuma de poliuretano e pasta.
De acordo com Opasanon et al. (2012), a pelicula consiste numa formulação complexa, que inclui cálcio e alginato de prata, combinados com água de ligação a 10 %. No caso da pasta, esta apresenta cerca de 40% de hidratação, consiste numa pasta amorfa e homogénea que se adapta bem ao leito da ferida, ajudando a evitar eventuais “espaços mortos” onde possam florescer bactérias e está indicada em feridas com pouco exsudado.
Quando a pelicula ou pasta entram em contacto com o exsudado da ferida, o fluido é absorvido pela matriz de alginato o que provova dilatação e suavização da matriz, fazendo com que as moléculas de prata e alginato de cálcio libertem os iões de prata para a ferida (figura 1), de acordo com Opasanon et al. (2012).

Figura 1: Acção da matriz de alginato com prata iónica (in: http://www.bbraun.com )
Dado que a matriz de alginato contém água de ligação na sua estrutura, a humidificação do produto antes da aplicação não é necessária, sendo que as experiências in vitro demonstraram que o efeito antimicrobiano tem início na primeira hora de utilização do penso, devido à disponibilidade de prata iónica.
De acordo com Opasanon et al. (2012) foi demonstrado in vitro que a difusão de iões de prata a partir da matriz produz uma concentração estável de iões de prata de cerca de 60 ppm (partes por milhão) ao longo de sete dias (Figura 2), sendo que comparativamente, tem sido sugerido que a concentração mínima necessária para obtenção de um efeito antimicrobiano deve ser de 20 a 40 ppm.

Figura 2: Libertação de prata, da matriz de alginato com prata iónica ( In : http://www.woundsinternational.com/pdf/ )
Estudos de Caso
A metodologia utilizada nestes estudos de caso, visa demonstrar os efeitos do antimicrobiano prata sob a forma de matriz de alginato de cálcio, no tratamento de infecção de feridas, em especial na feridas crónicas. Foram portanto realizados estudos de caso que procuraram evidenciar as vantagens de duas apresentações deste apósito. Para tal foi efectuada uma documentação do historial clínico do doente e caracterização da ferida, bem como monitorização da área desta, com recurso a planimetria digital, recorrendo à análise de fotos digitais no software OsiriX. Esse mesmo registo fotográfico serviu como base para uma avaliação mais qualitativa da evolução da ferida.
Caso n.º 1: Sr. A. O.
Homem de 72 anos de idade, com úlcera venosa infra-maleolar, na face interna da perna direita, desde há 7 meses. Foi avaliado o Indice de Pressão Tornozelo-Braço (IPTB), que era de 0,86, pelo que permite a utilização de terapia compressiva, que é indispensável para o controlo da insuficiência venosa do doente. O tratamento anterior consistia com hidrofibra com prata e compressas como apósito secundário + terapia compressiva de curta tracção. Apesar da utilização de um penso com prata e de também já ter sido utilizado com regularidade desde há cerca de 6 semanas, uma solução de limpeza com Betaina + PHMB, o que permite excluir a presença de biofilme, a evolução cicatricial continuava lenta. Assim optou-se pela utilização de um penso de prata iónica, com resultados muito satisfatórios, permitindo o encerramento da lesão em cerca de 1 semana (ver figuras 3 a 6).
Tratamento Implementado: Limpeza com PHMB+ betaina solução PHMB+Betaina gel “X” e hidrofibras com prata, de 23/3/2012 a 14/5/2012 + terapia compressiva. Em 14/5/2012, aplicou matriz de alginato de cálcio com prata em pelicula.

Figura 3: Ferida exsudativa, coberta de parcialmente com fibrina, no inicio do tratamento com surfactante e hidrofibras com prata.

Figura 4: Cerca de 1 mês e meio depois a ferida evoluiu favoravel mas lentamente, tem agora metade da área. Apresenta lesão satélite devida ao facto de o doente ter retirado e depois voltar a colocar mal as ligaduras de compressão, devido a prurido. Note-se que as lesões e pele perilesional foram irrigadas com iodopovidona pelo doente. Nesta ocasião opta-se pela pelicula de Alginato de Cálcio com Prata.

Figura 5 e 6: Cerca de 1 semana depois da aplicação da matriz de Alginato de Cálcio com Prata, tanto a lesão original como a lesão satélite estão cicatrizadas, o apósito secundário foi espuma de poliuretano.
Caso n.º 2: Sr. A. N.
Homem de 84 anos de idade, com lesão de etiologia traumática no pé esquerdo há cerca de 3 meses, apresenta mais especificamente: Lesão de cerca de 5 cm2 associada a: loca de 7 cm de profundidade em direcção ao arco plantar, uma segunda loca 5cm de profundidade em direcção à face interna do pé lateral ao tendão de Aquiles e uma terceira loca de 3cm de profundidade em direcção à face externa do pé, também lateral ao tendão de Aquiles. Tem ainda uma lesão satélite abaixo e ao lado, que comunica com a superior. Sem tecido necrótico visível (Figuras 7 a 8)
Apresenta exsudado muito elevado, viscoso, cheiro fétido, amarelo esverdeado. Fez ciprofloxacina sem grande efeito há cerca de uma semana, préviamente ao inicio dos tratamentos. Nesta fase ainda eram visiveis e palpáveis abcessos laterais e do arco plantar, coincidentes com as locas exploradas por sonda. Estes abcessos, laterais apesar da irrigação abundante com soro fisiológico, mantinham-se pouco alterados, pelo que foram efectuados 2 orificios de drenagem nas faces laterais do calcâneo, após punção com lâmina de bisturi, o que permitiu uma lavagem mais eficaz, com drenagem abundante de liquido purulento. Após remoção do exsudado purulento foram aplicadas compressas embebidas em solução de betaina + PHMB, nas locas, durante 20 minutos. Após este periodo de limpeza foi aplicado Gel “X” de betaina + PHMB e uma hidrofibra com prata. O penso secundário era um poliuretano de 20cmX20cm que ficava completamente saturado e extravasava em grande quantidade para a ligadura.


Figura 7 e 8: Aspecto inicial das lesões, que evidencia tecido de granulação muito infectado, escurecido sem brilho, altamente friável. Note-se na face lateral do pé posterior, celulite na região dos abcessos identificados. Após esta intervenção a melhoria foi pouco notória, embora ainda assim a quantidade de exsudado espesso tenha diminuido significativamente.
A 16 de Maio de 2012, a evolução era positiva, com ligeira redução do volume do exsudado, que ainda assim saturava a totalidade do poliuretano 20cmX20cm, embora fosse menos espesso e tivesse um cheiro menos intenso. Nesta ocasião tivemos disponível o penso matriz de alginato de cálcio com prata e decidimos testar a sua eficácia neste caso complexo (figuras 9 e 10).


Figura 9 e 10: Penso de matriz de Alginato de cálcio com prata (pelicula) aplicado In situ. Nesta faze volvidas cerca de 3 semanas de tratamento, nota-se ligeira redução de edema e dos sinais de celulite, apesar de as locas manterem as dimensões originais.O material foi aplicado na máxima extensão das locas e em todos os orificios existentes. Apesar da sua textura semi-rigida, este material ao fim de alguns minutos começa a dissolver-se com a temperatura corporal e exsudado e molda-se a toda a superficie da ferida, locas incluídas, o que é extremamente vantajoso.
A 18 de Maio de 2012, dois dias depois da primeira aplicação do novo apósito denota-se uma redução moderada do exsudado, passando o poliuretano de 20cmX20cm a estar com apenas cerca de 80% de saturação, cheiro menos fétido. O tecido de granulação que se mantinha ainda escurecido, passa a ter uma tonalidade visivelmente mais clara. Todo o apósito foi dissolvido, apenas se verificando alguns vestigios na espuma de poliuretano. A loca externa, está agora encerrada, sem permitir passagem de dedo (que antes permitia) ou mesmo pinça ou sonda.



Figuras 11,12 e 13
A 20 de Maio de 2013, apenas 4 dias depois da 1ª aplicação da matriz de alginato de cálcio com prata os resultados são evidentes, o exsudado é muito reduzido (cerca de 25% de saturação do poliuretano), mais fluído, seroso, orificios com drenagem também serosa reduzida. Sem odor perceptível. Loca da lesão principal, resume-se a 1 cm, marginal à parte superior desta das “9h às 2h”.Denota-se ligeira margem de tecido de epitelização no polo inferior da ferida. Lesões satélites mantidas, mas sem comunicação entre sí. (Figuras 14 a 16).


Figuras 14,15 e 16
A 28 de Maio de 2012, verifica-se que o apósito manteve-se integro desde a última realização de penso em lesão satélite, pelo que permanece no local. Por acumulação de depósitos de fibrina no tecido de granulação ao longo do tempo foi novamente aplicada solução de PHMB+Betaina (Figura 17). A lesão satélite inferior aumenta gradualmente devido a processo osteomielitico do calcâneo. Inicia Antibioticoterapia. Na lesão principal: tecido de granulação preenche toda a lesão até à superficie da pele, não sendo distinguível qualquer vestigio de existência de locas. Tecido de granulação saudável, vermelho vivo, brilhante. Neste ponto temos a infecção local da ferida controlada, apenas permanecendo a osteomielite do calcâneo.

A 30 de Maio de 2012, temos a lesão satélite original completamente cicatrizada. Lesão satélite inferior em evolução (maioritáriamente fibrina e osteófitos). Margem de cerca de 0,5 cm de tecido de epitelização no pólo inferior (figura 18).

A 11 de Junho de 2012, a lesão principal resume-se a uma “banda” de tecido de granulação de cerca de +/- 0,6 cm de largura, com retalho cutâneo (residual da loca original) sobreposto. Lesão osteomielítica do calcâneo com cerca de 50% da superficie coberta de tecido de granulação.Tem hiperqueratose satélite, sugestiva de osteófito subjacente (figura 19). Manteve tratamento em curso às duas lesões, sendo que em 15 de Julho se encontravam completamente encerradas (figura 20 e 21).



Caso n.º 3: Sra. C. F.
Mulher de 99 anos de idade, diabética tipo II, com úlcera por pressão, categoria IV, calcâneo esquerdo, em desbridamento autolitico desde há duas semanas. Tratamento anterior Hidrogel + hidrocolóide (c/ plantago) associado a desbridamento cortante conservador (técnica “slice”), visto a região dos calcâneos ser bastante sensível ao desbridamento cortante, que está contra indicado na maioria destes casos. A 9 de Junho de 2012, apresenta uma área moderada de tecido necrótico húmido, de coloração amarelada e sinais de infecção do compartimento superficial, como o tecido de granulação escurecido e friavel, sem brilho, cheiro fétido, com exsudado reduzido. Nesta fase seria oportuno iniciar um antimicrobiano tópico, pois denota-se desde já “wound-breakdown”, com destruição de tecido saudável perilesional devido à infecção. No entanto a maioria das opções disponiveis, principalmente no que respeita a pensos com prata, consistem em materiais altamente absorventes como hidrofibras, alginatos, hidroalginatos e espumas, que face ao tecido necrótico que ainda se verifica, iriam provocar a sua desidratação, em vez de incentivar a sua remoção por autólise em ambiente húmido. Em alternativa poderia pensar-se em utilizar uma compressa de poliamida não aderente com prata, pois não tem capacidade de absorção, no então seria uma medida com fraco impacto pois também esta opção não conseguiria dar continuidade ao processo de desbridamento em curso, nem tão pouco, por consequência conseguiria actuar através do tecido necrosado remanescente na superficie da ferida. Assim sendo, tendo em conta que a matriz de alginato de cálcio com prata em pasta possui cerca de 40% de água, e apesar da empresa que desenvolveu o produto não ter estudos concretos acerca da sua eventual acção no estímulo ao desbridamento autolitico, decidimos testar o comportamento do produto face a uma ferida infectada, com tecido necrosado húmido em moderada quantidade. Decidiu-se inclusive deixar o material aplicado durante uma semana. A evolução foi bastante favorável e foi de encontro às expectativas, revelando-se como um produto de eleiç\ao nestes casos específicos (figuras 22 a 25) Tratamento Implementado: Limpeza com PHMB + betaina solução (para mais fácil remoção de detritos) e matriz de prata iónica + alginato c/ 40% H2O, apresentação em pasta.





Caso n.º 4: Sra. C. P.
Mulher de 61 anos de idade, com úlcera venosa de localização pouco comum, na face anterior da perna esquerda, compartimento tendinoso anterior, desde há 8 meses. De acordo com a doente, apresentava nesse membro desde há vários meses edema perimaleolar, formando-se uma protuberância nessa zona, que a dada altura ficou ruborizada com mais calor que a restante pele circundante, originando prurido intenso e ardor. De acordo com a doente a ferida teve origem ao “coçar” a área afectada.
Era seguida no Centro de saúde da área de residência com tratamento pouco optimizado para a etiologia da úlcera e estado do leito da ferida. Como terapia compressiva tinha meia elástica de compressão 20 mmHg, sendo o tratamento local da ferida feito com Hidrofibras com prata desde há vários meses por apresentar exsudado de cheiro fétido e espesso. O tecido de granulação apresentava-se muito escurecido e sem brilho, altamente friável. Pele quente ao toque, com rubor perilesional e regional, mais compatível com eczema venoso, podendo excluir-se a hipotese de celulite. De acordo com a doente nunca tinha sido efectuado nenhum estudo por doppler do memebro inferior. O IPTB obtido foi de 0,93 tendo sido seleccionada a terapia compressiva de curta tracção, sendo o grande desafio efectuar uma redistribuição da pressão sub-ligadura de modo a abranger a área em questão, com pressão que surta efeitos terapêuticos. Normalmente essa área é uma das zonas da perna menos afectadas pela terapia compressiva, de acordo com a técnica que uso habitualmente, a técnica de Peter Staudinger, pelo que a solução passou por utilizar uma variante do cruzado em “8” no tornozelo, que permita evitar excesso de pressão e fricção durante a caminhada, que é indispensável quando se utiliza a terapia compressiva de curta tracção. A infecção local do leito da ferida era bastante severa, tal como descrito, sem grande resposta à terapêutica em curso (hidrofibras com prata), pelo que se optou por excluir a provável presença de biofilme e começar desde logo o tratamento com prata iónica, pois tem um inicio de acção mais rápido e uma maior disponibilidade de prata que o penso anteriormente utilizado, sendo que não havia tempo a perder no que respeita ao tratamento, visto que já estavamos perante várias áreas de “wound-breakdown”, pelo que a ferida estava a aumentar de tamanho desde há um mês de acordo com a doente. A evolução foi extremamente satisfatória e graças a um tratamento optimizado de acordo com o diagnóstico de situação efectuado a lesão cicatrizou no espaço de cerca de um mês, pondo fim a 8 meses de evolução e dor intensa (ver figuras 27 a 32).
Tratamento Implementado: Limpeza com PHMB + betaina solução, seguida de Matriz de alginato com prata iónica, em película, como apósito secundário foi utilizado uma espuma de poliuretano + terapia compressiva de curta tracção. Foi ainda aplicado um corticóide na pele perilesional. Nos últimos tratamentos, por apresentar pouco exsudado, optou-se por aplicar matriz de alginato com prata iónica em pasta.






Caso n.º 5: Sr. P. S.
Homem de 32 anos de idade, com história de Quisto dermóide sacro-coccigeo (Sinus Pilonidalis), desde há 12 meses com dois episódios de abcesso associados, faz Exerése do mesmo a 20 de Setembro de 2012, sem reconstrução por retalho, ficando loca cirúrgica para cicatrizar por segunda intenção. A ferida apresentava-se moderadamente exsudativa, com exsudado espesso, fétido e leito da ferido com tecido de granulação escurecido e friável. Dada a sua localização, considera-se como tendo grande risco de contaminação/infecção. Devido ao curto periodo de existência da lesão, a hipotese de apresentar biofilme é excluida apesar de apresentar depósitos de fibrina abundantes. A lesão estava a ser tratada com gaze impregnada em hidrogel e compressas como apósito secundário. Deu-se prioridade às aplicação de um apósito com prata iónica, de modo a controlar os níveis de contaminação/infecção e equilibrar o ambiente húmido com uma espuma de poliuretano. Considerando que estas lesões demoram cerca de 3 meses em média para cicatrizar, o facto desta lesão ter encerrado em apenas um mês, ilustra a eficácia do tratamento optimizado seleccionado para este caso (ver figuras 33 a 41)
Tratamento Implementado: Irrigação com soro fisiológico, seguida de Matriz de alginato com prata iónica, em pasta, com o objectivo de começar desde cedo a tratar a infecção, mas ao mesmo tempo optimizando o ambiente húmido de modo a facilitar o destacar da fibrina presente no leito da ferida + espuma de poliuretano. Os tratamentos seguintes incluiram Apósito de matriz de alginato com prata iónica em película + espuma de poliuretano.








Considerações Finais
Após a apresentação destes casos, emerge uma questão: haverá diferença entre os vários pensos com prata? Na nossa opinião a resposta é sem dúvida:sim!
Não falamos apenas no tipo de tecnologia utilizada na impregnação da prata no apósito, mas também do tipo de apósito utilizado, pois sabemos que classicamente os pensos com prata consistem na sua maioria em apósitos com material altamente absorvente, como é o caso de espumas de poliuretano, hidrofibras e fibras de alginato de cálcio, pois de facto a maioria das feridas é altamente exsudativa quando está infectada. No entanto quando a ferida está infectada, mas pouco exsudativa, a aplicação destes apósitos é contraproducente, pois vai deiquilibrar o ambiente húmido necessário à cicatrização da ferida e fomentar a deposição de fibrina na superficie da ferida. Assim para este tipo de feridas torna-se extremamente útil a aplicação de um apósito antimicrobiano com algum grau de hidratação como é o caso dos apósitos de matriz de alginato de cálcio com prata iónica, que tal como o nome indica, a prata já se encontra no estado iónico devido a essa hidratação, trazendo mais beneficios no tratamento da infecção. Assim, nem todos os antimicrobianos são úteis em todos os contextos.
Para cada caso específico deve ser seleccionado o antimicrobiano com o perfil mais adequado. O diagnóstico adequado de infecção na ferida e a selecção de um antimicrobiano ajustado, são um aspecto critico a não descurar.
A matriz de alginato com prata iónica permite uma libertação gradual e sustentada;
Após humedecimento com o exsudado as fracções da matriz espalham-se por todo o leito da ferida. Sob a forma de película apresenta hidratação de 10% liberta iões Ag+ quase de imediato e de forma contínua – libertação começa durante a 1ª hora de contacto e apresenta a maior concentração de prata iónica disponível,quando em comparação com os seus pares. Apresenta libertação sustentada ao longo de 7 dias, cerca de 60 partes por milhão (Opasanon et al., 2012)
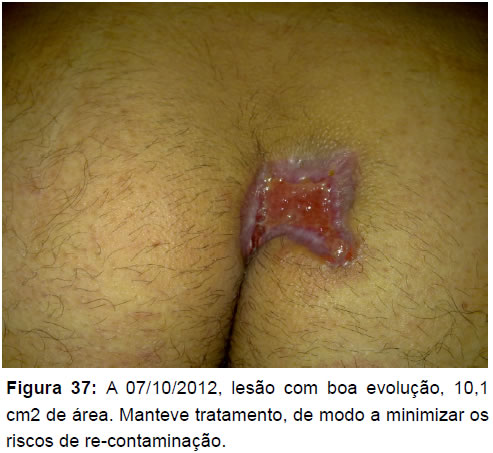
De facto olhando para os resultados obtidos, trata-se uma nova opção para o tratamento avançado de feridas, a ter sériamente em conta como opção na resolução de situações complexas, tal como no caso de úlceras de etiologia arterial, como o caso apresentado nas figuras 42 a 44.


Figura 43: Lesão 4 dias depois, com tecido de granulação vermelho vivo, menos pálido e com redução de 3,2 cm2 de área.
Referências Bibliográficas